细胞是生命活动的基本单位。每时每刻,人体内都在上演着大量不同类型细胞间交互作用所形成的交响曲。然而,在这一连接微观与宏观之间的介观尺度上,却存在巨大的技术空白,使得当前研究难以在哺乳动物的活体环境器官尺度下同时观测大量细胞在不同生理与病理状态下的时空异质性,极大限制了脑科学、免疫学、肿瘤学、药学等学科发展。仅以脑科学为例,大量神经元间的相互连接和作用涌现出如智能、意识等功能,厘清神经环路的结构和活动规律是解析大脑工作原理的必由之路。然而具备单神经元识别能力的传统显微镜往往只具备毫米级视场,仅能覆盖小鼠单个或几个脑区实现单个平面的神经信号动态记录;功能核磁虽然能够实现三维全脑范围观测,但空间分辨率却远不足以识别单细胞。因此,2013年启动的美国脑计划也将“大规模神经网络记录技术”列为九大资助领域之一。同样,对于肿瘤学而言,只有兼具大视场与高分辨才能全景式捕捉肿瘤发生发展的完整过程,从而更精准地研究不同药物反应,发现新的药物靶点。
瞄准这一国际前沿难题,清华大学戴琼海院士团队早在2013年就获得了国家自然科学基金委重大科研仪器研制项目支持,在国际上率先开展了介观活体显微成像领域研究,并于2018年成功研制了国际首台亿像素介观荧光显微仪器RUSH,能够同时兼具厘米级视场与亚细胞分辨率。尽管这一系统被国际同行誉为介观显微成像领域的先驱,但是由于仪器复杂昂贵,在当时仅能被少数科学家使用。与此同时,RUSH系统仍然面临一系列瓶颈,包括:如何利用二维传感器实现高速三维成像;如何避免激光长时间照射所引起的细胞损伤(即光毒性)从而实现长时程高速观测;如何克服复杂成像环境导致的光学像差与背景干扰;如何提升弱光条件下的成像信噪比;如何高效处理大规模介观数据等等。每一项技术瓶颈本身都是生物医学成像领域的国际难题,而如何在同一系统上同时解决这些活体成像壁垒,则变得更为挑战。
此后六年间,戴琼海院士带领成像与智能技术实验室,瞄准活体介观显微成像高峰,持续攻关这些国际前沿难题,先后提出扫描光场成像原理、数字自适应光学架构、虚拟扫描算法、共聚焦扫描光场架构、自监督去噪算法等关键理论与技术,相关成果均发表于《细胞》(Cell)、《自然》(Nature)、《自然·生物技术》(Nature Biotechnology)、《自然·方法》(Nature Methods)等国际期刊,逐一解决了介观活体显微成像中一系列壁垒,为新一代介观活体显微仪器奠定了基础。

图1.活体介观成像的技术空白
9月13日,清华大学戴琼海院士团队在《细胞》(Cell)发表最新工作:长时程活体介观成像完整记录哺乳动物器官尺度的三维细胞交互行为(Long-term mesoscale imaging of 3D intercellular dynamics across a mammalian organ),宣布了新一代介观活体显微仪器RUSH3D系统的问世,在兼具厘米级三维视场与亚细胞分辨率的同时,RUSH3D能以20Hz的高速三维成像速度实现长达数十小时的连续低光毒性观测。相比当前市场上最先进的商业化荧光显微镜,其在同样分辨率下的成像视场面积提升近百倍,三维成像速度提升数十倍,光毒性降低上百倍(有效观测时长提升百倍)。这一前所未有的跨空间和时间的多尺度成像能力,为复杂生物过程研究提供了全新视角。区别于传统光学显微镜聚焦于单个细胞内的物质交互过程,RUSH3D使得研究人员可以首次以全景方式动态观测哺乳动物器官尺度细胞精度的组织异质性,在活体组织中原位研究大规模多样化细胞在完整生理与病理过程中的动态交互行为。
交叉研究团队利用RUSH3D在脑科学、免疫学、医学与药学等多学科展示了令人瞩目的成果。首次在活体小鼠上以单细胞分辨率实现了覆盖大脑皮层2/3层的高速长时程三维观测,捕捉了多感官刺激下皮层各脑区的各异性响应模式,能够连续多天以单神经元精度追踪大规模神经响应。首次观测到了急性脑损伤后多脑区的免疫反应,发现大量中性粒细胞从非血管区域往脑内的迁移与回流过程。首次在小鼠免疫反应过程中同时观测到了淋巴结内多个生发中心的形成过程,以及T细胞在不同生发中心之间的迁移现象。这些初步实验虽然仅仅展现了RUSH3D应用的冰山一角,但充分展示了其为神经科学、免疫学、肿瘤学、药学等领域前沿研究所带来的广阔应用前景。该仪器的研制与产业化填补了对复杂生命现象介观尺度活体观测的空白,标志着我国在活体介观显微成像领域持续引领国际发展,极大提升了我国高端科研仪器的研究和应用水平,更为人类探索生命奥秘打开了新的维度,为揭示神经、肿瘤、免疫新现象和新机理提供了新的杀手锏,使得我国生命科学家、医学家能够率先使用我国自主高端仪器设备来解决重大基础研究问题。
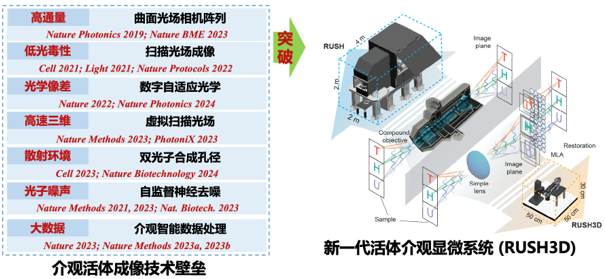
图2.RUSH3D系统图
计算成像是改变了传统光学成像“所见即所得”的设计理念。利用计算编码、计算采集等多维尺度计算架构,实现对高维光场的超精细感知与融合,为机器设计更好的感知系统,从而突破传统光学成像的一系列物理瓶颈。然而这条创新之路同样充满荆棘,RUSH3D系统集成了团队过去十多年来一系列的理论和关键技术创新,才真正实现了整体性能的颠覆性提升。针对二维传感器难以捕捉三维动态变化的难题,团队提出了扫描光场成像原理,能够在实现轴向400微米范围的高速三维成像的同时,将激光照射对细胞的损伤降低了数百倍。针对活体组织复杂环境引起的光学像差降低系统成像分辨率与信噪比这一难题,团队提出了基于波动光学的数字自适应光学架构,无需在光学系统中增加额外波前传感器或者空间调制器,在后端即可完成大视场多区域自适应光学像差矫正,从而提升大视场复杂环境三维成像的空间分辨率以及信噪比。这一设计使得仅需常规尺寸物镜,就能有效克服空间非一致的系统像差和样本像差难题,实现了全视场内均一高空间分辨率的十亿像素成像,显著降低介观成像系统尺寸与成本,使得高分辨活体介观显微成像系统变得更加广泛可及。除此之外,活体荧光成像中背景荧光严重影响了成像信背比,RUSH3D采用多尺度去背景算法实现背景信号和在焦信号的分离,精准滤除散焦背景,从而提升成像信背比,恢复淹没在荧光背景中的荧光信号。进一步与共聚焦扫描光场融合,将能在具备高通量介观观测能力的同时,实现共聚焦成像保真度。
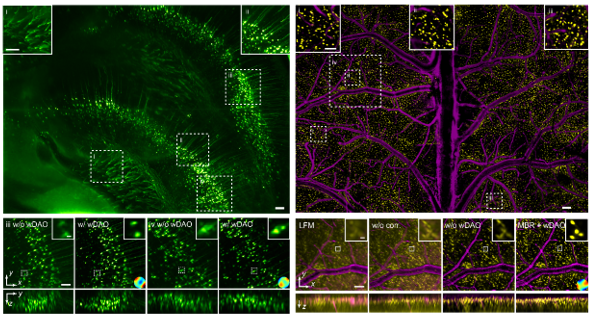
图3.RUSH3D实现大视场与高分辨率兼备的介观三维成像
RUSH3D通过其跨时空的多尺度成像能力,极大拓宽了科学家对大脑的认知。大脑皮层的神经元网络被认为是高等动物神经系统中十分重要而又复杂的信息处理中心,是产生生物智能乃至意识的关键神经网络区域。然而,由于观测技术限制,目前大部分研究只能同时记录实验动物中一个或几个皮层区域的神经元活动,难以进一步研究皮层神经元网络的联合动态变化。通过RUSH3D大视场、三维高分辨率、高帧率的成像优势,交叉团队开创性实现了对头固定下清醒小鼠背侧皮层17个脑区中十万量级大规模神经元的长时间高速三维记录,并且能够对同一群神经元进行跨天连续的追踪。运用该系统,证实了响应感觉刺激,调控运动的神经元并非只存在于单一感觉皮层、运动皮层,而是广泛存在于皮层各个区域,但各个区域神经元对感觉信息编码、整合、区分的能力存在差异。进一步发现自发运动行为发起时,小鼠皮层神经元网络由尾侧向鼻侧传导的发放模式。这一结果提示视觉、触觉等感觉皮层神经元的信息整合和全皮层范围信号扩散可能是引起自发运动的关键因素。在此基础上,RUSH3D有望首次实现解析全背侧皮层的介观脑功能图谱,通过捕捉大脑内的成百上千万神经元间的动态连接与功能,有望能揭示意识的生物学基础,智能的本质等人类基本问题,推动对神经退行性疾病的研究,并有望推动脑启发的人工智能发展。
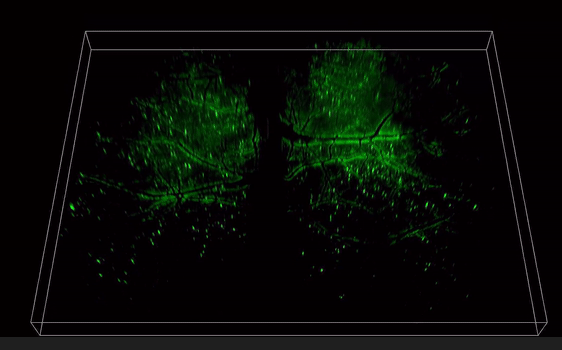
图4.小鼠全脑皮层范围三维神经成像
RUSH3D系统为研究大规模细胞交互提供了前所未有的工具。例如,生发中心(Germinal center, GC)是被抗原激活后的B细胞在趋化作用引导下聚集形成的组织结构,对于自身免疫性疾病、疫苗、病毒感染等过程都至关重要。由于受到视场和拍摄时长的限制,免疫细胞如何参与多个GC生成以及如何在多个GC间进行迁移的过程从来没有被连续记录过,从而限制了该领域的发展。团队利用RUSH3D对小鼠腹股沟附近淋巴结在免疫反应85个小时左右进行了长达十数小时的高速三维成像,完整记录了B细胞参与多个GC生成的过程。与此同时,观测到在免疫反应145个小时GC已经完全形成之后,一些T细胞在多个GC之间完整迁移的过程,预示了T细胞可能参与了GC之间的信息交流和传递。这些对信使T细胞在不同生发中心之间交流信息的观测有望带来我们对免疫过程的全新认识。
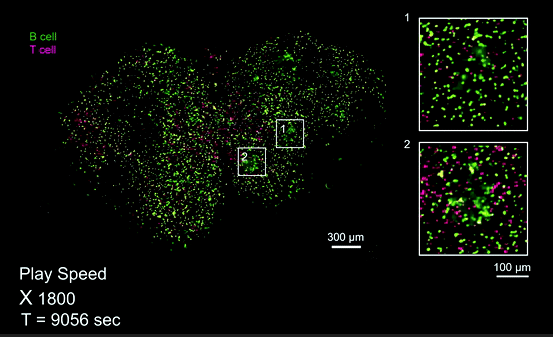
图5.B淋巴细胞参与小鼠淋巴结多个生发中心形成的完整过程
跨时空的多尺度成像能力使得RUSH3D极大提升了实验效率。例如,药物筛选实验能够在单次实验中显著提高效率,免去多次试验需求。同时,由于RUSH3D可以提供足够数据进行统计分析,跨个体差异可以在一次实验中得到有效缓解。此外,诸如肿瘤转移等稀有事件,在RUSH3D的观察中将不再是偶发事件,而是常规可见现象,成百上千倍地提升了活体生物发现的效率。凭借其低光毒性三维观测的优势,该系统还能够同时观察到细胞间的长距离通信,并通过长时间追踪数百万个细胞,揭示集体细胞行为的物理规律和功能涌现的机制,例如能够捕捉从肿瘤发生开始到免疫应答、肿瘤生长的全过程,揭示肿瘤产生的完整免疫活化反应。作为RUSH3D在医学领域的初探,研究人员首次观测到了急性脑损伤(脑震荡等)后整个大脑皮层范围内的中性粒细胞迁移活动。当小鼠的脑部受到撞击以后,大量的中心粒细胞从血管周边非血管区域流出进入脑实质,也有极罕见的细胞从脑实质回流到血管里,这意味着有些细胞可能通过类淋巴系统进入脑实质,并且会流回血管中将信息传递到生物体的其他地方。通过国际首次捕捉对脑损伤修复过程单细胞水平的免疫反应,有助于开发特定疗法避免急性脑损伤后组织水肿带来的脑功能缺失难题,并为更广泛的脑疾病等医学问题提供新视角。
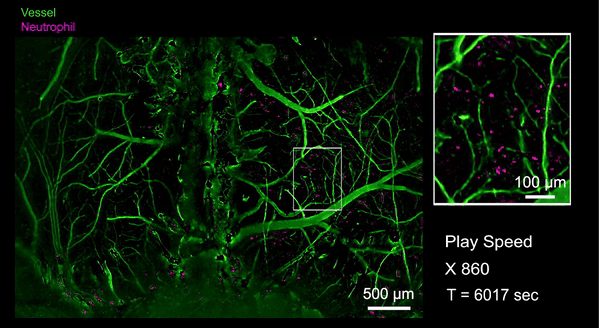
图6.急性脑损伤后全皮层范围单细胞水平免疫反应
基于该系列成果的核心专利已于清华大学转化成立了国产自主先进显微仪器公司,致力于国产自主可控具备国际领先性能的高端光学显微镜以及其在生命科学等领域的前沿应用。已支撑清华、北大、北航、北师大、解放军总医院、同济医院等国内高水平科研机构,在肿瘤学、免疫学、脑科学等不同领域开展了20余项创新性生命科学研究,服务于生物制药领域。
清华大学自动化系博士后张元龙、深圳国际研究生院博士生王鸣瑞和基础医学院博士生朱齐禹是本文共同第一作者,清华大学自动化系戴琼海院士、吴嘉敏副教授,基础医学院郭增才副教授为论文共同通讯作者,郭钰铎、刘波、李嘉敏、姚啸、孔垂、张亿、黄予超、祁海参与并作出重要贡献。研究得到国家自然科学基金委、国家科技部重点研发计划以及清华大学Brain-X项目的大力支持。
论文链接:
https://doi.org/10.1016/j.cell.2024.08.026
① 凡本站注明“稿件来源:中国教育在线”的所有文字、图片和音视频稿件,版权均属本网所有,任何媒体、网站或个人未经本网协议授权不得转载、链接、转贴或以其他方式复制发表。已经本站协议授权的媒体、网站,在下载使用时必须注明“稿件来源:中国教育在线”,违者本站将依法追究责任。
② 本站注明稿件来源为其他媒体的文/图等稿件均为转载稿,本站转载出于非商业性的教育和科研之目的,并不意味着赞同其观点或证实其内容的真实性。如转载稿涉及版权等问题,请作者在两周内速来电或来函联系。





 中国教育在线
中国教育在线



