肝癌是全球癌症相关死亡的第三大原因,手术切除后的复发率高达70%,如何准确预测肝癌复发是一个难题。中国科学技术大学孙成研究组与合作者开发了预测肝癌复发的“TIMES”评分系统,通过量化免疫细胞在肿瘤微环境中的空间分布特征,实现了对肝细胞癌复发风险的预测,准确率达82.2%。他们将科学成果直接转化为可应用的AI诊断工具——公开免费的TIMES在线版本,上传病理染色图像即可获得肝癌复发风险评分。北京时间3月13日0点,该项成果发表在国际学术期刊《自然》上。
“TIMES”评分系统全称为“Tumor Immune MicroEnvironment Spatial”(肿瘤免疫微环境空间)评分系统,是首个结合空间免疫信息的肝癌复发预测工具。研究证明了免疫细胞的空间分布比其整体数量更能决定临床预后,将空间转录组学、蛋白质组学和多光谱免疫组化技术与人工智能驱动的空间分析整合,创造了肿瘤微环境评估的全新方法。
肿瘤微环境的空间异质性表现为不同肿瘤区域呈现差异化的免疫细胞组成。自然杀伤细胞(NK细胞)作为先天免疫系统的关键效应细胞,已有临床数据提示肿瘤内NK细胞浸润程度升高与患者生存预后显著相关。然而,当前临床评估体系主要依赖肿瘤特征的常规组织病理学分层方法,尚未整合免疫细胞在肿瘤微环境中的空间分布参数及其对预后的潜在影响。研究团队发现CD57+NK细胞亚群在肿瘤微环境中的空间定位具有特殊的预后意义:肿瘤侵袭前缘区域CD57+NK细胞密度增高的患者表现出显著降低的复发风险。
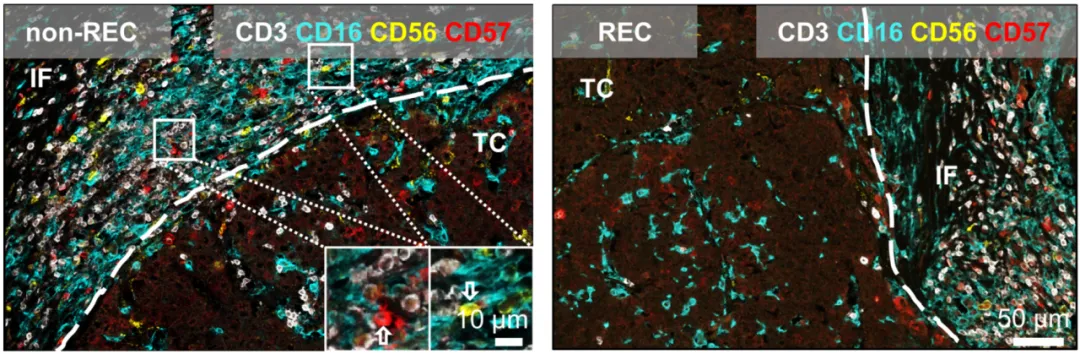
非复发(non-REC)和复发(REC)组织中的多色免疫组化染色。与复发肝癌相比,非复发肝癌患者的肿瘤侵袭前缘区域(invasive front)NK细胞更为丰富。
如何解释NK细胞的分布与肝癌复发有关?研究团队基于61名患者的肝癌切片进行了系统性的转录组-空间组学整合分析,解析多重免疫荧光高维数据,应用梯度增强机器学习算法模型鉴定了SPON2、ZFP36L2、ZFP36、VIM和HLA-DRB1这五个具有显著预后意义的基因标记物,它们作为五个基本指标,构成了能有效预测肝癌复发的算法模型TIMES评分系统。
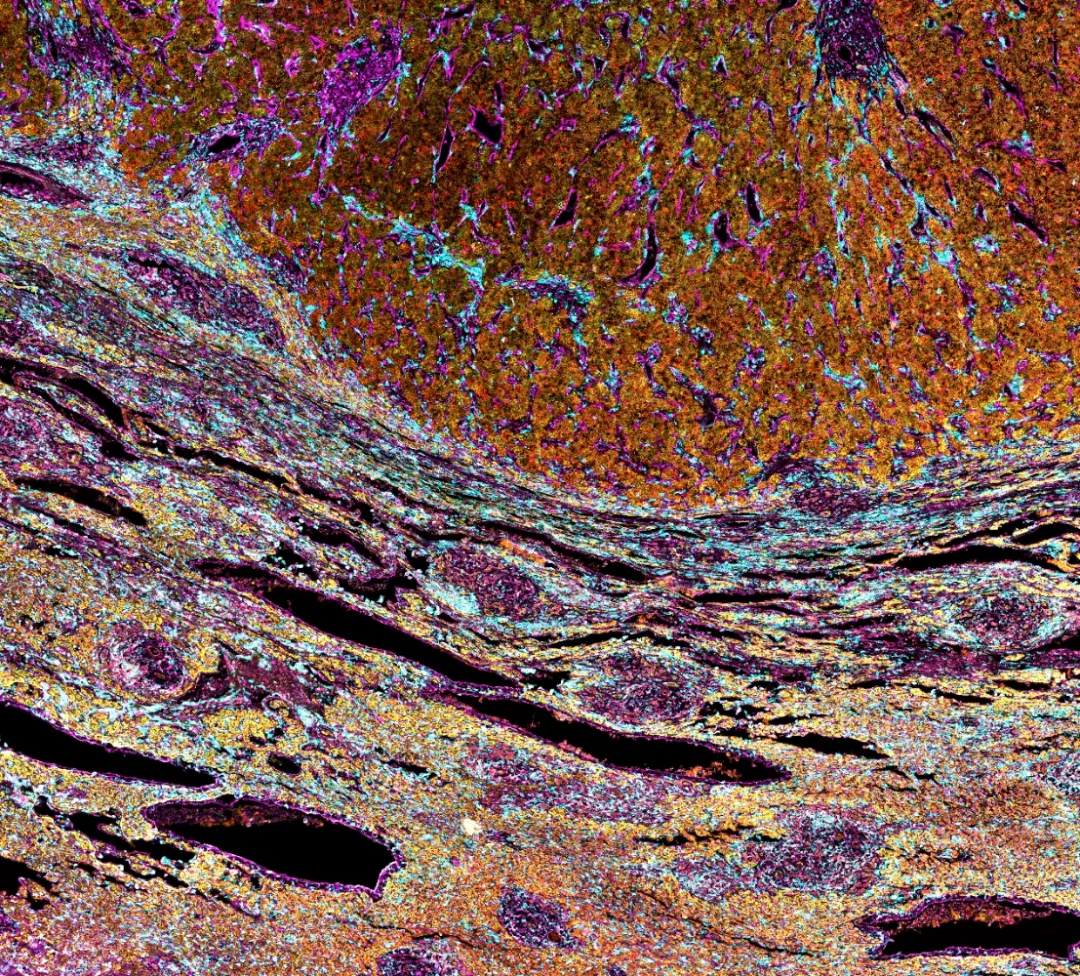
复发组织的代表性多色免疫组化图像,显示核染色(DAPI,蓝色)和生物标志物:CD57(红色),SPON2(绿色),HLA-DR(青色),ZFP36L2(黄色),ZFP36(橙色)和VIM(洋红色)。
在231位患者的多中心验证研究中,TIMES评分系统区分非复发和复发组织的准确率为82.2%,现有的肝癌临床分期系统,如巴塞罗那分期、TNM分期系统的预测准确率在50%左右。
SPON2指标在TIMES评分系统中是最具预测性的。研究团队针对SPON2指标的生物学意义开展了进步研究,通过3D打印实验、杀伤实验等,发现SPON2促进NK细胞的运动和向肿瘤细胞的定向运动,SPON2阳性NK细胞表现出更强的细胞毒性,并显著增加细胞毒性T淋巴细胞的活化。随后,研究者进一步建立NK细胞上SPON2特异性敲除小鼠的肝癌复发模型,发现SPON2增强免疫调节蛋白IFN-γ分泌和NK细胞浸润,可以明显抑制肿瘤的进展。这些说明SPON2阳性NK细胞能够降低肝癌的复发风险。
为了方便临床社区访问TIMES系统,团队开发了全球可用的在线网络平台(https://sun.times.ustc.edu.cn/),上传患者肝癌组织的标准病理染色图像或数据,即可获得带有TIMES评分和复发风险的报告。TIMES系统相关的核心算法和模型已获得专利保护,研究团队正积极寻求与企业合作,推动该预测系统的规范化临床转化应用。研究团队希望能够提供全新的临床决策辅助工具,帮助医生在有限资源条件下为患者制定最优化治疗方案,让预测肝癌复发的TIMES系统普惠可及。
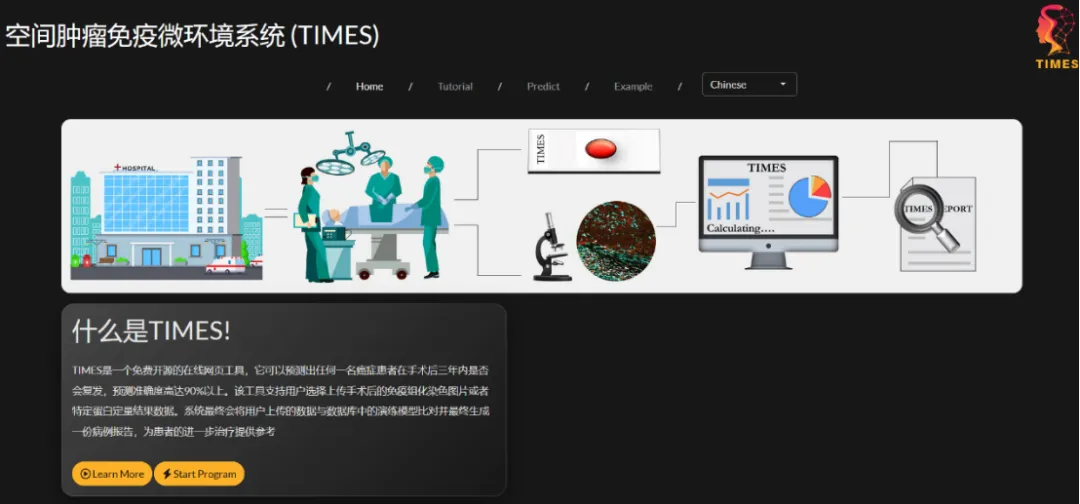
TIMES在线网络平台(https://sun.times.ustc.edu.cn/)
匹兹堡大学免疫治疗领域知名专家Michael T. Lotze教授为该研究撰写了深入的科学述评,强调这项研究“提供了令人信服的证据,证明空间免疫构架在肝细胞癌预后评估中具有首要地位”(provides compelling evidence for the primacy of spatial immune contexture in prognosticatings hepatocellular carcinoma),“建立了一个方法学框架,可广泛应用于实体肿瘤,通过精确的空间免疫分析指导免疫治疗干预”(establishes a methodological framework that could be broadly applicable across solid tumor malignancies, potentially guiding immunotherapeutic interventions through precise spatial immune profiling)。
中国科学技术大学孙成教授、中国科学技术大学刘连新教授、新加坡科学技术研究局Joe Yeong教授为本文的共同通讯作者;贾耿介教授(中国农科院基因组所)、贺培崎博士(中国科学技术大学)、戴天力博士生(中国科学技术大学)、Denise Goh研究员(新加坡科学技术研究局) 为本文的共同第一作者。该工作还得到了其他团队成员的大力帮助。
论文链接:https://www.nature.com/articles/s41586-025-08668-x
① 凡本站注明“稿件来源:中国教育在线”的所有文字、图片和音视频稿件,版权均属本网所有,任何媒体、网站或个人未经本网协议授权不得转载、链接、转贴或以其他方式复制发表。已经本站协议授权的媒体、网站,在下载使用时必须注明“稿件来源:中国教育在线”,违者本站将依法追究责任。
② 本站注明稿件来源为其他媒体的文/图等稿件均为转载稿,本站转载出于非商业性的教育和科研之目的,并不意味着赞同其观点或证实其内容的真实性。如转载稿涉及版权等问题,请作者在两周内速来电或来函联系。





 中国教育在线
中国教育在线



